 撰文:Vergil 编辑:RNAScript 排版:三姐夫 为了主动将LNP靶向特定细胞类型,人们将大量工作集中在修饰LNP的脂质组成上或用靶向基团(包括配体和抗体片段)赋予表面功能化。然而,脂质偶联物使LNP的生产复杂化,阻碍了相关制剂的放大生产和临床转化。在LNP生产过程中掺入修饰也会同时导致靶向配体的封装,从而降低纳米颗粒表面靶标结合位点的可用性,而额外的功能化配体附着也可能以错误的方向发生。尽管这些LNP修饰可以改善靶组织积累和受体介导的内化,但它们也会同时改变LNP表面电荷,增加纳米颗粒尺寸,并改变蛋白质吸附曲线,从而导致生物分布、摄取和免疫原性的改变。 2024年10月17日,昆士兰大学BASE研究所Seth W.Cheetham教授团队在预印本bioRxiv上传了题为“Targeted mRNA delivery with bispecific antibodies that tether LNPs to cell-surface markers”的研究论文。在这项研究中,团队考虑到抗体偶联修饰LNP这一靶向递送思路面临的相关困境,开发了一种单独注射的双特异性抗体(BsAb)靶向剂。施用后与靶细胞表面蛋白结合,起到连接LNP和靶细胞的桥梁作用。 本研究中展示了mRNA-LNP向表皮生长因子受体(EGFR)和叶酸水解酶1(PSMA)阳性细胞的高效和特异性递送。该技术通过取代BsAb的细胞靶向区域实现的灵活性,使下一代靶向mRNA药物的快速开发成为可能。  双特异性抗体靶向剂的验证 双特异性抗体(BsAb)包含两个单链可变片段(scFv),它们可以与LNP外部的PEG和靶细胞表面富集的蛋白质结合。细胞特异性mRNA-LNP递送可以通过在给药前将BsAb以预混合的方式通过非共价连接到LNP表面来实现(图1a),或通过预靶向(图1b),优先使细胞暴露于BsAbs,然后施用未修饰的LNP实现。 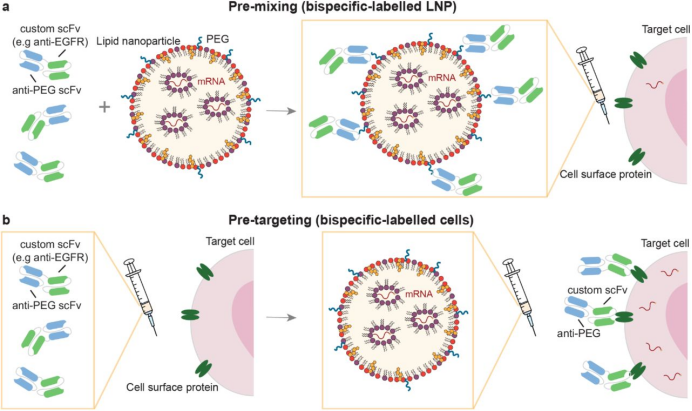 图1. 双特异性抗体靶向设计思路 为了将预靶向这一分别给药mRNA-LNP和BsAb的方式与常见的预混合方式进行比较,研究首先表征了将靶向剂连接到LNP(预混合)对LNP特性的影响。mRNA-LNP与BsAb的预混合使抗PSMA和抗EGFR BsAb的mRNA-LNP中位大小分别从82 nm增加到181 nm和412 nm(图2a)。BsAb修饰改变了LNP形态,降低了颗粒均匀性并诱导聚集(图2a,b),这些变化可能会影响LNP在体内的行为。 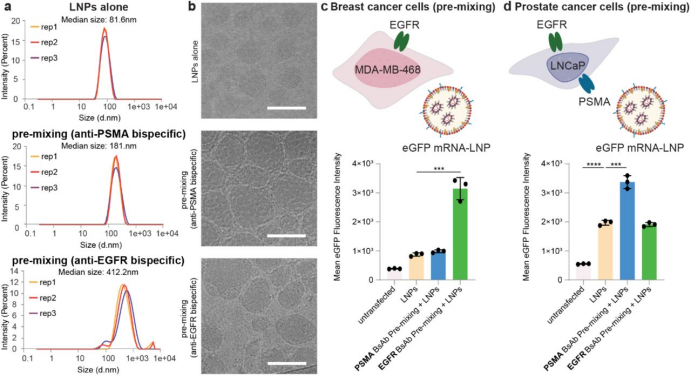 图2. 细胞与双特异性抗体的预混合会改变mRNA-LNP的物理化学性质和递送 体外验证 接下来,研究使用了仅表达表皮生长因子受体(EGFR)但不表达叶酸水解酶1(PSMA)的MDA-MB-468乳腺癌细胞,以及同时表达EGFR和PSMA的LNCaP前列腺癌细胞进行特异性递送效果的评估。LNP结合EGFR+PEG BsAbs的预混合增强了mRNA-LNP向MDA-MB-468的递送(图2c)。当mRNA-LNP与PSMA+PEG BsAb预混合时,eGFP mRNA-LNP在LNCaP前列腺癌细胞中的递送显著改善。与非靶向LNP相比,EGFR+PEG BsAbs预混合对eGFP表达没有影响(图2d)。 在此基础上,将实验结果与BsAbs预靶向细胞进行了比较。与预混合相比,用EGFR+PEG BsAbs预靶向MDA-MB-468乳腺癌细胞显著增加了eGFP表达近4倍,比未修饰mRNA-LNP提高12倍(图3a,b)。同样,PSMA BsAbs对LNCaP前列腺癌细胞的预靶向使eGFP表达提高了近3倍(图3c,d)。与非靶向LNP转染相比,PSMA+PEG预靶向实现了5倍的eGFP表达。值得注意的是,EGFR+PEG BsAbs的预靶向增强了mRNA-LNP向LNCaP细胞的递送,而预混合并没有提高摄取。 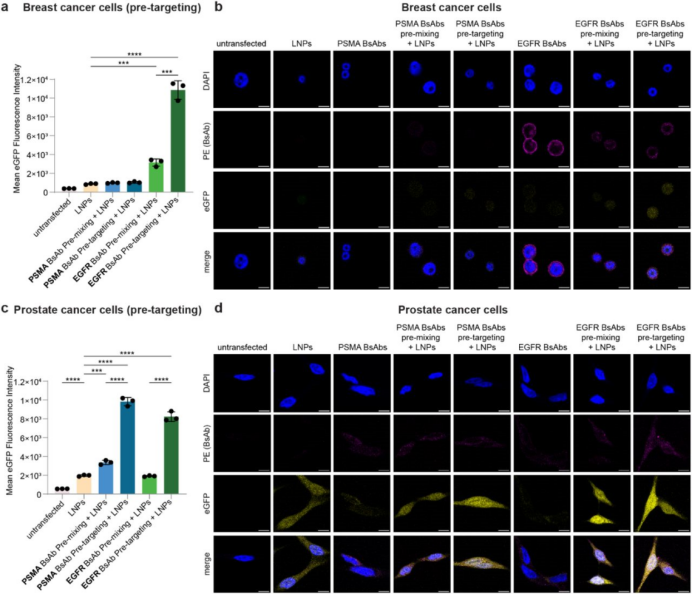 图3. 预靶向策略可改善mRNA-LNP的细胞特异性递送 总之,与BsAbs的预混合和预靶向有助于细胞类型特异性mRNA-LNP的体外递送。预靶向方法适用于不同的细胞系和靶抗原,并且比预混合更有效。主动靶向利用与细胞表面受体的相互作用,通过内吞作用促进特异性和内化。由于BsAb的大小范围低于触发受体介导的内吞作用,使得它们积累在质膜上,并在mRNA-LNP结合后被内化(图3b,d)。预靶向策略除了可以保持mRNA-LNP的理化性质外,与预混合中LNP上并不丰富的PEG相比,预靶向细胞表面可用的BsAb结合位点更多,增加的亲和力可能会改善递送。 体内验证 由于用EGFR-PEG BsAbs预靶向MDA-MB-468在体外比非靶向和预混合LNP递送取得了最大的改善,研究人员进一步在体内测试了这种情况。通过静脉内给药向皮下接种MDA-MB-468异种移植物的BALB/c裸鼠模型注射萤火虫荧光素酶mRNA-LNP(图4a)。给药后8小时,与非靶向LNP相比,EGFR-PEG BsAbs 的预混合和预靶向分别将递送到肿瘤组织的mRNA-LNP增加了8倍和7倍以上,同时将肝脏中的发光分别减少了1/3和1/2(图4b)。48小时后,所有实验组的肝脏荧光素酶表达均降低,相比之下,预靶向的小鼠中的发光较8小时仅降低了约10%,而预混合组肿瘤的发光降低了60%(图4c)。 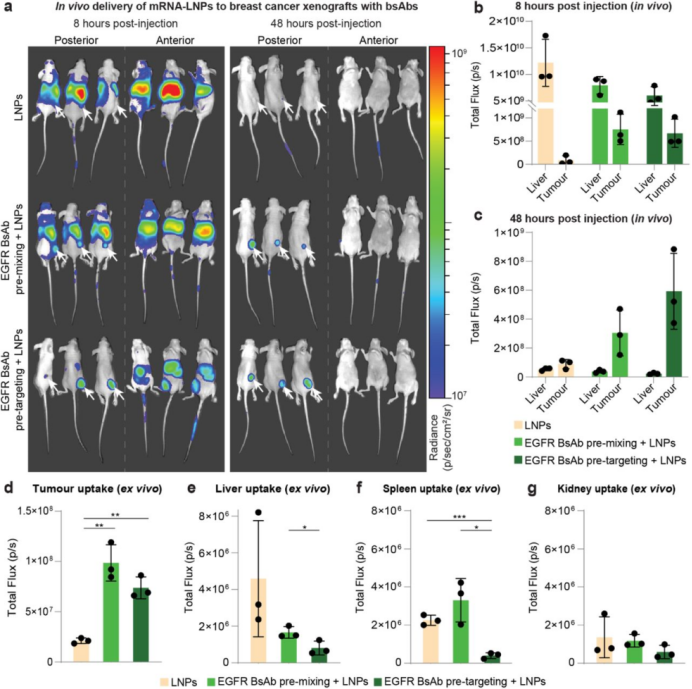 图4. 预靶向策略改善体内mRNA-LNP的靶向递送 肿瘤组织离体分析显示,预混合和预靶向之间的发光相当,与非靶向mRNA-LNP给药相比,发光率分别提高了4.6倍和3.5倍以上(图4d)。此外,非靶向LNP组的肝脏总通量最高,而预靶向小鼠肝脏中的总通量显著降低(图4e)。脾脏信号显示,预靶向小鼠的脾脏摄取最低(图4f)。预混合BsAbs LNP的高脾摄取可能是由于理化性质的变化,包括LNP周围聚集的蛋白冠以及电荷改变。 体内实验证明,预靶向策略的mRNA-LNP在肿瘤中的表达效率高于预混合的靶向方式,同时进一步降低了药物在肝脏和脾脏中的表达信号。 总结 对LNP和细胞表面标志物具有特异性的BsAb在体外和体内展示了有效的mRNA-LNP靶向。通过预靶向将BsAb和纳米颗粒给药分离实现了优异的mRNA摄取和表达。与预混合策略相比,预靶向可以减少血清附着的蛋白质污染对颗粒表面的影响,从而改善mRNA-LNP的生物分布,减少脱靶效应,继而减少剂量以降低mRNA疗法的毒性。 与功能化mRNA-LNP相比,mRNA-LNP和靶向试剂(BsAb)的单独给药方式大大简化了生产。mRNA-LNP偶联BsAbs的成熟临床应用和安全性也为本技术简化临床转化提供了强有力的先例,有望推动实现下一代mRNA药物的快速开发,以应对蛋白质替代疗法和基因编辑的应用挑战。 然而,体内注射靶向剂的稳定性、靶向准确性和安全性决定了这一策略的临床应用潜力,仍是值得探讨的问题。能否通过该策略实现mRNA-LNP药物更好的靶向性有待进一步的研究。 参考资料 https://www.biorxiv.org/content/10.1101/2024.10.17.618962v1.full-text 为促进mRNA治疗领域的合作交流,我们组建了专业的mRNA行业交流群,目前院校、企事业单位的各路精英已纷纷加入,如果您也想加入交流学习,不要犹豫哦~ 长按下方二维码,添加主编微信进群。由于申请人数较多,添加微信时请备注:院校/企事业单位名称—专业/职务—姓名。如果您是PI/教授/研发骨干/主管及以上职务,还请注明。  往期推荐  Moderna第三季度财报业绩超预期,将全面推进mRNA呼吸道疫苗组合全球上市批准 达冕生物/华兰疫苗RSV mRNA疫苗IND申请获CDE受理 中检院 | 基于HPLC表征circRNA纯度、杂质和降解产物 尧唐生物开发非抗体偶联骨髓靶向LNP递送系统,实现高效安全的体内ABE mRNA递送和基因编辑 克服黄病毒抗体依赖性增强,单剂量circRNA疫苗有效预防寨卡/登革热病毒感染 吕雪光团队开发LNP电荷辅助稳定策略,维持雾化制剂稳定性,助力mRNA吸入疫苗/疗法开发 巴斯德研究所发起全球mRNA疫苗合作倡议 BioNTech发布第三季度财报,披露旗下3款mRNA肿瘤疫苗最新进展 里程碑!辉大基因获得FDA首次批准CRISPR/Cas13 RNA编辑疗法HG202,用于治疗黄斑变性 嘉晨西海自复制RNA肿瘤治疗药物JCXH-211+ICIs组合疗法获批临床试验! 聚焦mRNA治疗领域行业发展 |